Ejercicio
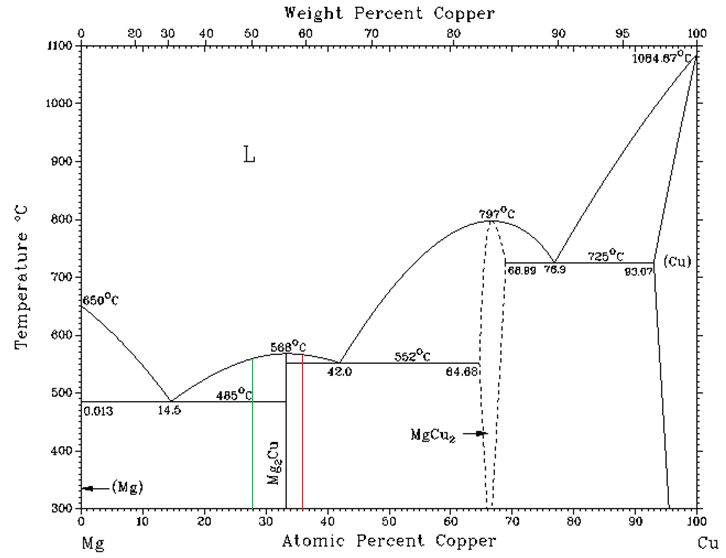
De respuesta a los siguientes requerimientos acorde con el diagrama de fases Mg-Cu:
1. Calcule la cantidad de microconstituyente proeutéctico que existe a 551.99°C en una aleación que contiene 64% Mg.
2. Calcule la composición química de la aleación hipereutéctica que a 485.01°C formará la misma cantidad de proeutéctico que usted halló en el numeral 1.
3. Calcule las cantidades de microconstituyentes eutécticos que existirán a 300°C para la aleación que halló en el numeral 2.
Desarrollo
Punto 1. Una aleación que contiene 64% Mg posee 36% Cu (la suma debe ser igual a 100% de aleación). La cantidad de microconstituyente proeutéctico o primario se calcula usando la regla de la palanca, con el brazo a la derecha del fulcro de la misma. Así:
$$ \%Mg_2 Cu_{proeutéctico} = \frac{(42-36)\%Cu}{(42-33.5)\%Cu} \times 100\% = 70.59\%~Mg_2 Cu_{proeutéctico} $$
Punto 2. La cantidad de proeutéctico que hallamos en el numeral 1 es \( 70.59\%~Mg_2 Cu_{proeutéctico} \), luego, la composición química de la aleación se obtiene de emplear la regla de la palanca aplicada para el cálculo de la cantidad de fase del compuesto \(Mg_2Cu_{proeutéctico}\):
$$ 70.59\%~Mg_2 Cu_{proeutéctico} = \frac{X-14.5}{33.5-14.5} \times 100\% = 27.91 \% Cu$$
La composición de la aleación es, entonces, \(Mg\)-\(27.91\%Cu\).
Punto 3. Para la composición de la aleación hallada en el numeral 2 ya se posee una cantidad de microconstituyente proeutéctico, el cual fue calculado en el numeral 1, que es:
$$ 70.59\%~Mg_2 Cu_{proeutéctico} $$
La cantidad de fase líquida antes de producirse la reacción eutéctica (es decir, justo por encima de la temperatura de la reacción eutéctica) es:
$$ \%L = 100\% - 70.59\%~Mg_2 Cu_{proeutéctico} = 29.41 \%L$$
Al producirse la reacción eutéctica este 29.41%L se transformará en dos fases sólidas que conformarán el microconstituyente eutéctico, así:
$$ 29.41\%L = \%Mg_{eutéctico} + \% Mg_2Cu_{eutéctico} $$
Ec. 1
Ahora, la clave para calcular los microconstituyentes eutécticos consiste en tener en cuenta que el microconstituyente primario o proeutéctico corresponde al compuesto \(Mg_2Cu\). Por esta razón, es conveniente calcular primero, usando la regla de la palanca, el porcentaje de fase \(Mg\) del microconstituyente eutéctico, es decir:
$$ \%Mg_{eutéctico} = \frac{33.5-27.91}{33.5-0} \times 100\% = 16.69 \%Mg_{eutéctico} $$
Por último, se calcula el porcentaje de \(Mg_2Cu\) que hace parte del microconstituyente eutéctico como la diferencia entre la cantidad de fase líquida antes de la reacción eutéctica y la cantidad de fase \(Mg_{eutéctico}\), dado que sabemos que dicha fase líquida reaccionará y se transformará por completo en el microconstituyente eutéctico (recordar la Ec.1), luego:
$$ \%Mg_2Cu_{eutéctico} = 29.41\%L - 16.69\% Mg_{eutéctico} = 12.72\%Mg_2Cu_{eutéctico} $$




Comentarios potenciados por CComment